阿司匹林肠溶片人体生物等效性研究分析
发布时间:
2023-06-05
来源:

一、背景
阿司匹林的发现,起源于柳树。最早在公元前1534年,古埃及的医药文献《埃伯斯医药典》记载了古埃及人使用柳树来消炎镇痛。公元前400年,希腊医生希波克拉底用柳树叶煎茶来给妇女服用以减轻分娩的痛苦。1758年英国Edward Stone教士发现晒干的柳树皮对疟疾的发热、肌痛、头痛症状有效。到了19世纪初期,随着技术革新、科学进步和生产发展,柳树皮消炎镇痛的有效成分被发现。1852年,蒙彼利埃大学化学教授Charles Gerhart发现了水杨酸分子结构,并首次用化学方法合成水杨酸。1876年,John Maclagan在《柳叶刀》上发表了首个含有水杨酸盐类的临床研究,该研究发现水杨苷能缓解风湿患者的发热和关节炎症。1897年德国化学家Felix Hoffman通过修饰水杨酸合成了高纯度的乙酰水杨酸,乙酰水杨酸很快通过了对疼痛、炎症及发热的临床疗效测试。直到1899年,拜耳才注册并销售了一种名为乙酰水杨酸的改良版本,商品名为“阿司匹林”。至此,阿司匹林作为非处方止痛药问世。
阿司匹林早期作为解热镇痛药进入临床使用,我国于1958年开始生产。到目前为止,已应用百年,成为医药史上三大经典药物之一,曾是世界上应用最广泛的解热、镇痛和抗炎药。近年来发现阿司匹林对血小板聚集有抑制作用,能阻止血栓形成,临床上用于预防短暂脑缺血发作、心肌梗死、人工心脏瓣膜和静脉瘘或其他手术后血栓的形成,特别在预防心脑血管疾病方面应用广泛,在心绞痛、急性心肌梗死、缺血性脑卒中、短暂性脑缺血发作、经皮冠脉介入及外周动脉病的一、二级预防中,具有不可替代的、举足轻重的作用。阿司匹林作为防治心脑血管不良事件的“基石”地位已被多项循证医学研究结果所确立。
因为阿司匹林的自身性状,国外市售的阿司匹林剂型种类很多,以片剂为主,包括普通片、肠溶片、颗粒剂、泡腾片等,也有软膏剂,阿司匹林肠溶和奥美拉唑速释的复方制剂,微粉阿司匹林片等。国内已申报的阿司匹林品种亦十分丰富,有速释剂型包括普通片、泡腾片、胶囊剂、散剂、栓剂等,有肠溶制剂包括肠溶片和肠溶胶囊,有缓释制剂包括缓释片和缓释胶囊,还有注射制剂、各种复方制剂和前体药物制剂等。
阿司匹林的口服固体制剂最常见的不良反应是胃肠道症状,因为口服阿司匹林会剌激胃黏膜而引起上腹部不适及恶心呕吐。而把阿司匹林制成肠溶制剂可避免药物对胃的直接刺激,也防止药物在胃内分解失效,控制药物在肠道内定位释放。因此,普通阿司匹林片的临床应用胃肠道不良反应发生率高,阿司匹林肠溶片的安全性比较高。所以,可以说阿司匹林新剂型中应用最广的当属阿司匹林肠溶片。
本文将结合相关指导原则和文献研究,详细阐述阿司匹林肠溶片(100 mg和300 mg)临床研究的一般考虑,对本品人体生物等效性研究的若干关键设计进行探讨,旨在为此类产品的仿制和注册申报提供参考。
二、药物简介
通用名称:阿司匹林肠溶片
商品名称:Aspirin/Bayaspirin
英文名称:Aspirin Enteric-coated Tablets
化学结构式:
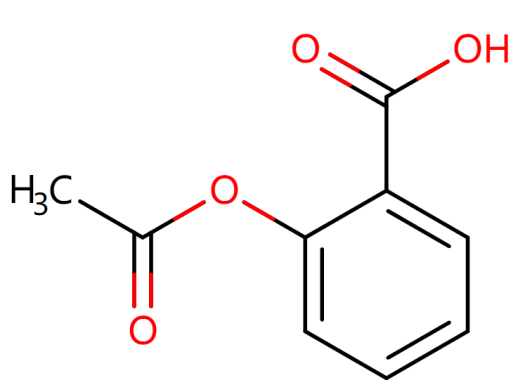
辅料:
规格:100 mg、300 mg
适应症:阿司匹林对血小板聚集的抑制作用,因此阿司匹林肠溶片适应症如下:降低急性心肌梗死疑似患者的发病风险、预防心肌梗死复发、中风的二级预防降低短暂性脑缺血发作(TIA)及其继发脑卒中的风险、降低稳定性和不稳定性心绞痛患者的发病风险、动脉外科手术或介入手术后,如经皮冠脉腔内成形术(PTCA),冠状动脉旁路术(CABG)、颈动脉内膜剥离术,动静脉分流术、预防大手术后深静脉血栓和肺栓塞、降低心血管危险因素者(冠心病家族史、糖尿病、血脂异常、高血压、肥胖、抽烟史、年龄大于50岁者)心肌梗死发作的风险。
用法用量:口服,每天100-300 mg
1、理化性质

2、溶出情况
作为肠溶制剂,阿司匹林肠溶片定位于肠道中释放,其在各PH条件下的溶出情况显著影响体内试验的结果,因此通过体外溶出试验分析受试制剂与参比制剂的溶出一致性显得尤为重要。《中国药典2020版》要求阿司匹林肠溶片在PH 1.0的条件下2 h溶出量应小于标示量的10%,转到pH 6.8 缓冲液中45 min的溶出量应大于标示量的70%。
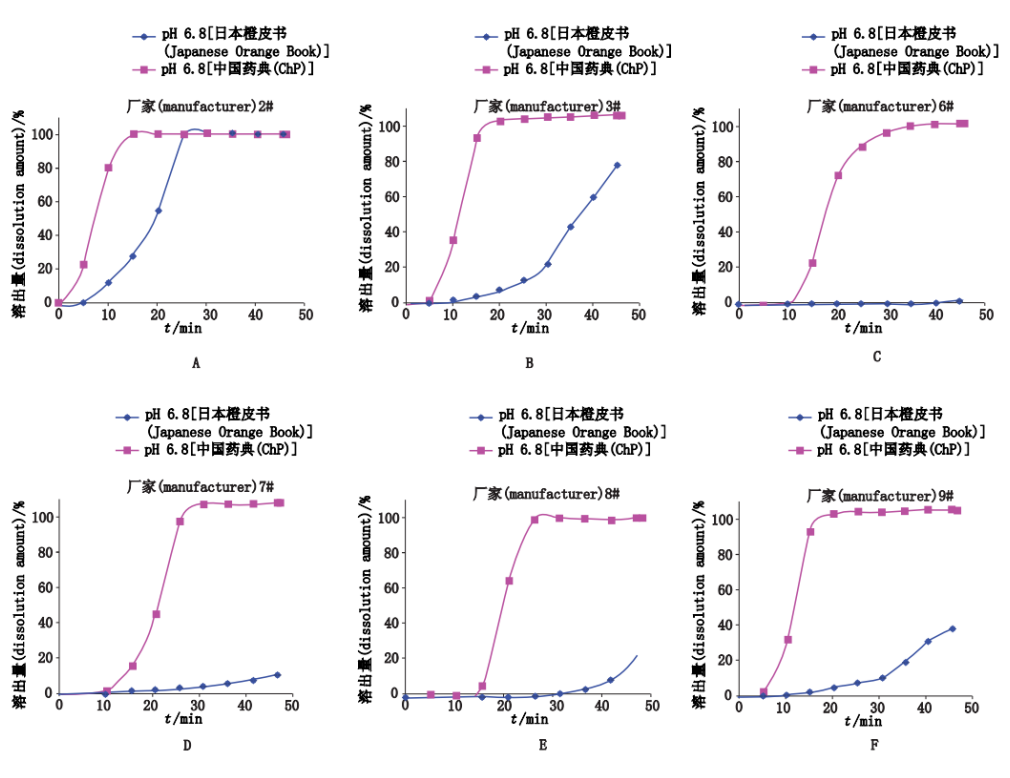
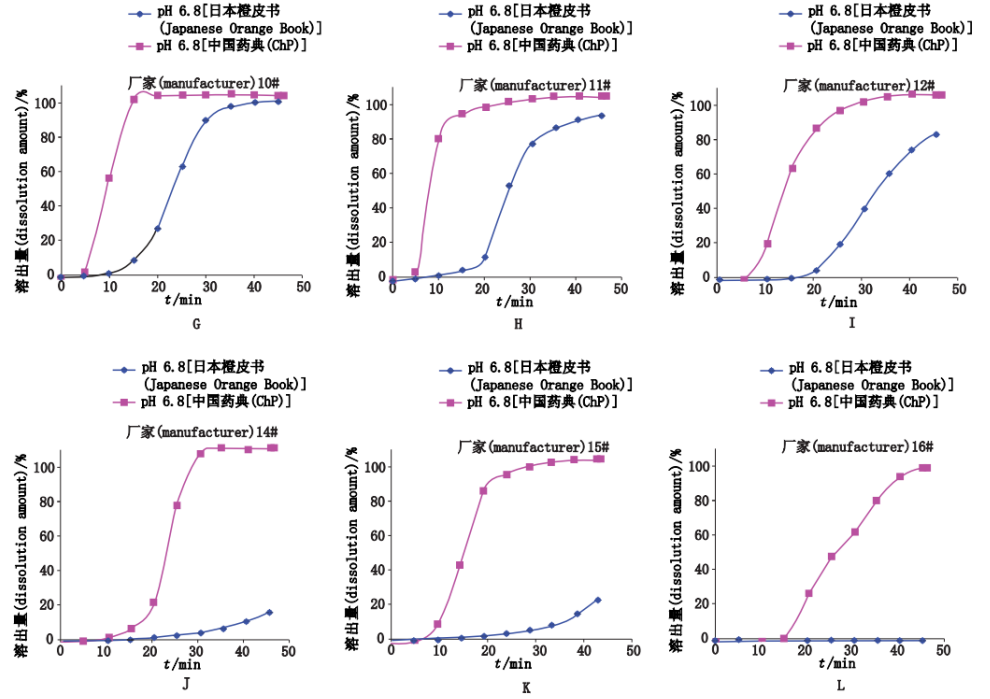
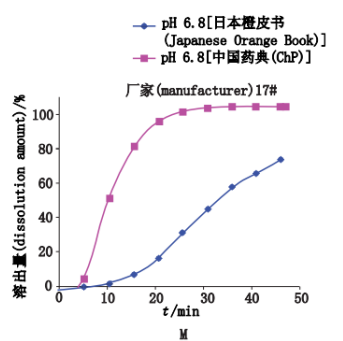
刘洁[1]等人测定了多个厂家的阿司匹林肠溶片在pH 6.8(中国药典2010年版)、pH 6.8(日本橙皮书)介质中的实时释放曲线,结果如下图所示。由于以中国药典2010年版二部的方法制备的pH 6.8缓冲液离子强度为日本橙皮书的方法制备的pH 6.8缓冲液的2至3倍,且离子种类也不一致,2种释放介质中释放曲线数据差异较大,提示溶出介质中的离子种类和离子强度对受试样品的溶出行为有较大的影响。
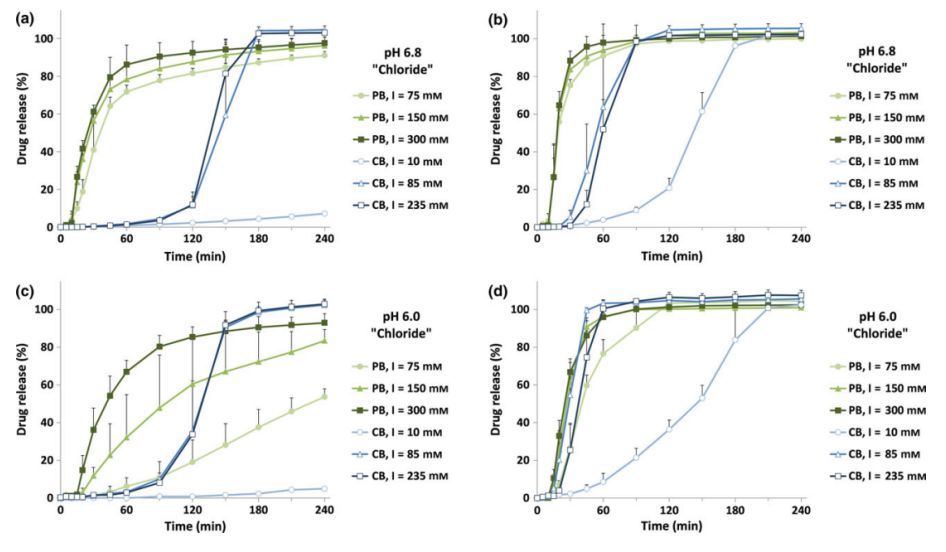
Frank Karkossa和Sandra Klein[2]比较了肠溶衣(EC)阿司匹林制剂在不同pH、电解质组成和离子强度的磷酸盐和碳酸氢盐缓冲溶液中的药物释放情况。结果如下图所示,发现EC阿司匹林制剂的药物释放受到缓冲物质和离子强度的影响。在所有缓冲溶液中,药物释放随着离子强度的增加而增加,但与磷酸盐缓冲液相比,碳酸氢盐缓冲液的药物释放延迟。有趣的是,溶出介质中的阳离子种类对药物释放也有明显的影响。在模拟小肠液pH和平均离子组成的新缓冲溶液Blank CarbSIF中获得的药物释放曲线与在研究的所有其他缓冲液组合物中获得的药物释放曲线不同,提示在进行溶出试验时,尽可能模拟腔内液体的离子组成。
Frank Karkossa和Sandra Klein[2]比较了肠溶衣(EC)阿司匹林制剂在不同pH、电解质组成和离子强度的磷酸盐和碳酸氢盐缓冲溶液中的药物释放情况。结果如下图所示,发现EC阿司匹林制剂的药物释放受到缓冲物质和离子强度的影响。在所有缓冲溶液中,药物释放随着离子强度的增加而增加,但与磷酸盐缓冲液相比,碳酸氢盐缓冲液的药物释放延迟。有趣的是,溶出介质中的阳离子种类对药物释放也有明显的影响。在模拟小肠液pH和平均离子组成的新缓冲溶液Blank CarbSIF中获得的药物释放曲线与在研究的所有其他缓冲液组合物中获得的药物释放曲线不同,提示在进行溶出试验时,尽可能模拟腔内液体的离子组成。
三、生物等效性评价
1、总体设计
CDE于2022年10月发布的《阿司匹林肠溶片生物等效性研究技术指导原则》,建议采用两序列、两周期、交叉试验设计,也可采用重复交叉设计,开展单次给药的空腹及餐后人体生物等效性研究。
一项CDE公布的一致性评价企业研究报告及生物等效性试验数据信息公开如下表所示:
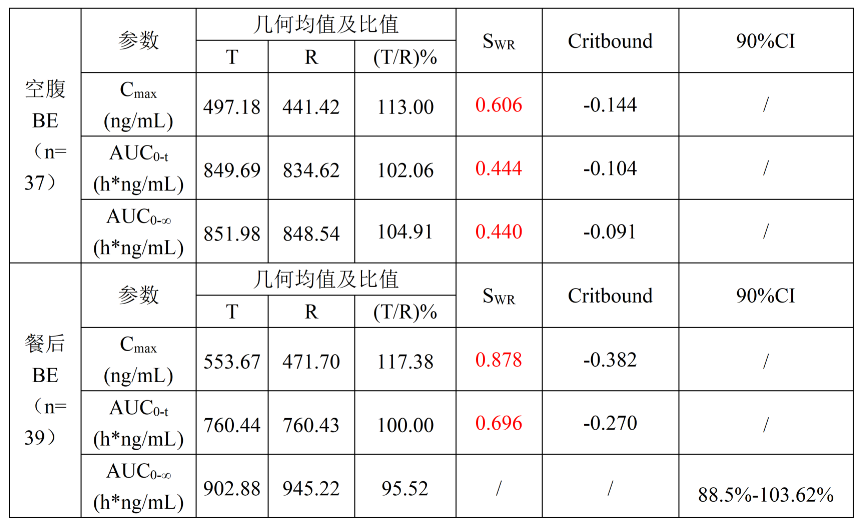
阿司匹林肠溶片由于其递送机制导致生物利用度受损,吸收延迟且不稳定,阿司匹林肠溶片与食物一起服用会导致吸收更不稳定,因此阿司匹林在空腹和餐后状态下个体内变异均较大。正如上表所示,空腹和餐后状态下的Cmax和AUC0-t的个体内变异系数均远超过30%,因此更推荐采用重复交叉设计。
2、血样采集
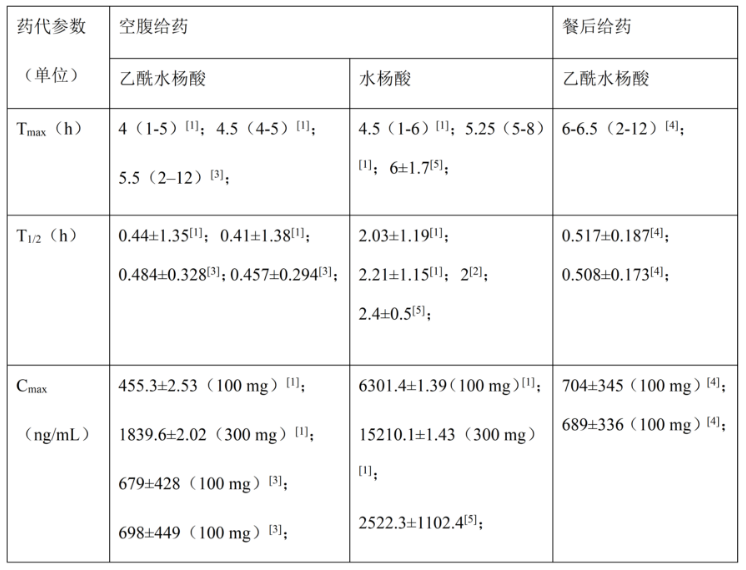
根据上述PK参数,BE研究采血点设计时需同时关注乙酰水杨酸和水杨酸的达峰时间范围以及半衰期,科学地设计采血点以满足生物等效性研究的需要。根据原研相关资料和文献数据,乙酰水杨酸空腹和餐后的Tmax中位值集中在4~6.5h,极值范围为1-12 h;水杨酸空腹的Tmax中位值集中在4.5~6h,极值范围为1-8 h,血浆中乙酰水杨酸和水杨酸的达峰时间不同,建议合理设计样品采集时间点同时兼顾两者的达峰时间。乙酰水杨酸和水杨酸半衰期的均值范围分别为0.41~0.517 h和2~2.4 h,本品经CYP2C9代谢,CYP2C9具有基因多态性,设计采血终点时需考虑慢代谢人群,在7个t1/2的基础上适当延长,因此采血终点可设计为24 h,既可满足法规对于采血终点不短于3个末端消除半衰期的要求,又能覆盖到吸收、分布与消除相。另外,本品经P-gP转运,试验期间注意避免使用中、强效P-gP抑制剂或诱导剂。
3、检测物质
根据《以药动学参数为终点评价指标的化学药物仿制药人体生物等效性试验指导原则》,一般推荐仅测定原形药物,对于从原形药物直接代谢产生的主要代谢产物,当代谢产物主要产生于进入体循环以前,并且代谢产物显著影响药物的安全性和有效性时,应测定该代谢产物。建议以原形药物评价生物等效性,代谢产物的相关数据用于进一步支持临床疗效的可比性。
乙酰水杨酸在吸收前,吸收中和吸收后迅速转化为其主要代谢物水杨酸,乙酰水杨酸半衰期短,在血液中不易检测。FDA阿司匹林缓释胶囊剂的个药指导原则及CDE发布的《阿司匹林肠溶片生物等效性研究技术指导原则》均推荐对血浆当中的乙酰水杨酸和水杨酸的血药浓度进行测量以进行生物等效性评价分析,因此本品生物等效性研究中的检测物质为血浆中的原型药物乙酰水杨酸及其代谢产物水杨酸。
四、生物等效性评价
建议以乙酰水杨酸的Cmax、AUC0-t和AUC0-∞作为生物等效性评价的指标,水杨酸的Cmax、AUC0-t和AUC0-∞用于进一步支持临床疗效的可比性。
若选择两序列、两周期、交叉试验设计,应采用平均生物等效性方法评价,受试制剂与参比制剂的Cmax、AUC0-t、AUC0-∞几何均值比值的90%置信区间应在80.00%~125.00%范围内。
若选择重复交叉设计,当SWR≥0.294,即CVW%≥30%,可采用RSABE方法进行等效性评价(应用于AUC、Cmax两者之中任意一个或全部采用)。当SWR<0.294,即CVW%<30%,则应采用ABE方法评价生物等效性。若的单侧95%置信区间上限小于等于零,同时,主要药动学参数的几何均值比(Geometric mean ratio, GMR)的点估计值在80.00%~125.00%范围内,可判定受试制剂与参比制剂的药动学评价指标(AUC或Cmax)具有生物等效性。
五、国内申报情况分析
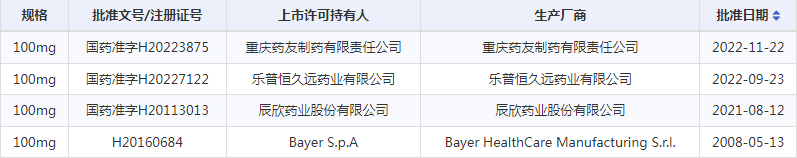
原研2003年11月06日于国内首次获得批准上市,目前有超过150家公司的阿司匹林制剂在国内批准上市,可谓“规格多,品种全,竞争激烈”。对于阿司匹林肠溶片,2015年后一共有37家公司进行了生物等效性试验备案登记,但迄今只有辰欣药业、乐普恒久远药业、重庆药友制药先后以化药4类报产该药并同通过一致性评价,反映出阿司匹林肠溶片的一致性评价难度较大。综合分析目前该品种在CDE登记的临床试验信息,所有申报生产的企业空腹和餐后试验多采用四周期、两序列完全重复交叉设计,样本量为54~90例(空腹+餐后,2×4)不等,提示本品BE试验样本量与两制剂间差异以及个体内变异相关,开展体内BE研究前应充分评估制剂差异,临床试验过程中应注重个体内变异控制,提高临床试验质量。
六、总结
我司完成了包括奥美拉唑镁肠溶片、奥美拉唑肠溶胶囊、雷贝拉唑钠肠溶片、艾司奥美拉唑肠溶干混悬剂、艾司奥美拉唑镁肠溶胶囊、度洛西汀肠溶胶囊等在内的多项正式BE研究,在肠溶制剂BE研究的方案设计和临床执行中亦拥有非常丰富的经验,帮助众多申办者完成了肠溶制剂品种的注册申报。我司拥有丰富的高难度药物及肠溶制剂药物的BE项目经验,其中高变异药物BE研究项目备案总数占全国同类产品20.21%,完成100余项高变异药物一致性评价,擅长根据特征指导药学关键溶出曲线的选择,提高研发效率。
七、参考文献
[1]刘洁,刘辉.阿司匹林肠溶片质量研究与分析[J].药物分析杂志,2015,35(12):2187-2192.DOI:10.16155/j.0254-1793.2015.22.
[2]Karkossa Frank,Klein Sandra,Assessing the influence of media composition and ionic strength on drug release from commercial immediate-release and enteric-coated aspirin tablets.[J] .J Pharm Pharmacol, 2017, 69: 1327-1340.
[3]Bayaspirin IF文件
[4]Bayaspirin德语说明书
[5]Wang Lu,Di Yujing,Guo Tingting et al. Implementation of a Reference-Scaled Average Bioequivalence Approach for Highly Variable Acetylsalicylic Acid in Fixed-Dose Combination with Clopidogrel Versus Enteric Aspirin in Chinese Subjects Under Fasting Conditions: A Phase 1, Open-Label, Randomized, Crossover Study.[J] .Adv Ther, 2020, 37: 2696-2709.
[6]Li Yan,Ming Jeffrey E,Kong Fangyuan et al. Bioequivalence Study Comparing Fixed-Dose Combination of Clopidogrel and Aspirin with Coadministration of Individual Formulations in Chinese Subjects Under Fed Conditions: A Phase I, Open-Label, Randomized, Crossover Study.[J] .Adv Ther, 2020, 37: 4660-4674.
[7]高志峰,赵媛媛,周杰.阿司匹林肠溶片生物等效性试验[J].药物分析杂志,2016,36(02):217-225.DOI:10.16155/j.0254-1793.2016.02.05.
预知更多品种分析,请咨询↓↓↓



